建築物の環境衛生10
建築物衛生行政概論 建築物の環境衛生 空気環境の調整建築物の構造概論 給水及び排水の管理 清掃 ねずみ・昆虫等の防除
単位集 水質検査項目及び特定建築物の水質検査頻度 法令集 法改正 参考資料
建築物の環境衛生⑩
水溶液の計算問題
1年から2年の周期に水溶液の計算問題が出題されます。
ここで、少し問題を解く際のポイントを記載いたします。
まず、水溶液の濃度の表し方には2種類あります。
- (溶質の質量[g] / (水溶液の質量[g]) x 100 = 水溶液の濃度[%]
- (溶質の質量[mg] / (水溶液の体積[L] = 水溶液の濃度[mg/L]
上記事柄は覚えましょう。
難しいようですが、つまり質量[g]を元の水溶液から割ってそれに100でかけるか、
質量を体積で割るかだけの問題です。
ビル管の試験の水溶液の問題はこれだけわかっておけばいいので、覚えましょう。
また、ここでの水溶液の密度もほぼ水の密度と等しいので、
水の密度:
- 1kg / L
- 1mLは1g
は覚えましょう。
令和5年度問題45
5%溶液の次亜塩素酸ナトリウムを水で希釈して200mg/Lの濃度の溶液を10L作る場合、必要となる5%溶液の量として、最も近いものは次のうちどれか。
- 0.4mL
- 2mL
- 4mL
- 20mL
- 40mL
解答
200mg/Lの溶液10Lに含まれる次亜塩素酸ナトリウムの量は
200[mg/L] x 10[L] = 2000[mg]=2[g]
必要となる5%溶液の量は
2[g] ÷ 0.05=40[g]
ここで
溶液1gは1mLなので
40[g]=40[mL]
になります。
令和3年度問題44
5%溶液として市販されている次亜塩素酸ナトリウムを水で希釈して100mg/Lの濃度の溶液を10L作る場合、必要となる5%溶液の量として、最も近いものは次のうちどれか。
- 0.2mL
- 4mL
- 20mL
- 40mL
- 200mL
解答
ここで、少し問題を解く際のポイントを記載いたします。
まず、水溶液の濃度の表し方には2種類あります。
- (溶質の質量[g] / (水溶液の質量[g]) x 100 = 水溶液の濃度[%]
- (溶質の質量[mg] / (水溶液の体積[L] = 水溶液の濃度[mg/L]
まず、100mg/Lの濃度の溶液を10L作る場合なので
実際に必要な次亜塩素酸ナトリウムは
100mg/L x 10L = 1000mg
になります。
そこで単位が
mg/L x LなのでLが約分されてmgが残り
1000mgになります。
1000mg = 1mLとみなしてよく
この1mLが全体の5%を占めてるので、全体は1mL ÷0.05 = 20mLになります。
令和元年度問題45
6%次亜塩素酸ナトリウム100mLを水30Lに加えた場合、この濃度の次亜塩素酸ナトリウム濃度に最も近いものは次のうちどれか。
- 20mg/L
- 60mg/L
- 100mg/L
- 200mg/L
- 300mg/L
解答
この問題の解答枠の単位をまず確認するとmg/Lです。
つまりmgをLで割ると答えがわかります。
問題文よりLは30Lと既に表れております。
従ってmgを問題文より導いてやれば答えが見えてくると思います。
問題文より
6%次亜塩素酸ナトリウム100mLは0.06 x 100 = 6mL
1mLは1gより
6mL = 6g
6g = 6000mg
になります。
従って
6000mg/30L=200mg/L
になります。
平成30年度問題45
5%溶液として市販されている次亜塩素酸ナトリウム16mLに水を加え、およそ20mg/Lの濃度に希釈するときに加える水の量として、最も近いものは次のうちどれか。
- 0.8L
- 3.2L
- 4L
- 32L
- 40L
解答
この問題も上記ポイントを理解したうえで答えを導きましょう。
まず、解答枠の単位がLです。問題からLを導きましょう。
次亜塩素酸ナトリウム16mLの5%溶液なので
16 x 0.05 =0.8mL
上記ポイントより
mL = g
従って
800mg ÷ 20mg/L = 40L になります。
平成26年度問題45
2.5%溶液として販売されている次亜塩素酸ナトリウムを適当量とって水100Lに加えたところ、できた溶液の濃度は30mg/Lになった。
最初にとった次亜塩素酸ナトリウム溶液の量に最も近いものは次のうちどれか。
- 8mL
- 12mL
- 40mL
- 80mL
- 120mL
解答
出来た溶液の濃度が30mg/Lで、水100Lを加えたわけだから
30mg/L x 100L = 3000mgになる。
ここでのポイントは単位に注意!
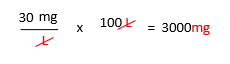
これは、覚えましょう。 上記水の密度は1mLは1gなので
3000mg = 3mL(1L = 1000g)
になります。 2.5%で販売されていた次亜塩素酸ナトリウムなので3mL(次亜塩素酸の量)に2.5%(0.025)で割ることで最初にとった次亜塩素酸ナトリウムの量を求めることが出来ます。
3mL / 0.025 = 120mLになります、
答えは5平成25年度問題45
5%溶液の次亜塩素酸ナトリウムを水で希釈して200mg/Lの濃度の溶液を10L作る場合、必要となる5%溶液の量として、最も近いものは次のうちどれか。
- 0.4mL
- 2mL
- 4mL
- 20mL
- 40mL
解答
まず、希釈後の溶質の量を求める。
200mg/Lの濃度の水溶液を10L作るわけだから200mg/L x 10L = 2000mg(1000mg=1g)より2[g]になります。
希釈前の水溶液の質量は
2 / 0.05 = 40[g]
になります。
今回は体積[mL]を求められているので
水の密度=1g / mLより
40mLになります。
答えは5
平成24年度問題45
5%溶液として市販されている次亜塩素酸ナトリウム100mLを水50Lに加えた場合、この溶液の次亜塩素酸ナトリウム濃度に最も 近いものは次のうちどれか。
- 10mg/L
- 50mg/L
- 100mg/L
- 500mg/L
- 1,000mg/L
解答
まず、5%溶液100mLに含まれる正味の次亜塩素酸ナトリウムの質量[mg]を求める。
水の密度の問題から
1mL = 1g
であるから、100mL = 100gである。
100g x 0.05(5%) =5[g]=5000[mg]
である。
希釈後の水溶液の濃度[mg/L]は
5000[mg] / 50[L] = 100[mg/L]
答えは3
である。この水溶液の計算の問題のポイントは解答枠の単位にも注目した方がいいでしょう。
今回の問題の単位は
mg/Lです。
つまり質量[mg]と体積[L]が解れば質量/体積で答えが解ることになります。
平成23年度問題45
5%溶液として市販されている次亜塩素酸ナトリウム50mLに適当な量の水を加えて、25mg/Lの濃度に希釈したい。加える水の量として、最も近いものは次のうちどれか。
- 10L
- 20L
- 50L
- 100L
- 200L
解答
希釈前の溶質の質量[mg]は
水の密度の問題から
1mL = 1g
であるから、50mL = 50gである。
50[g] x 0.05(5%) = 2.5[g] = 2500[mg]である。
従って
2500[mg] / 25[mg/L] = 100[L]
である。
ここでのポイントも解答枠の単位に[L]になっています。
問題では水を加えて、25mg/Lの濃度に希釈したいとあります。
そこで、解答枠体積[L]を導くためには質量[mg]が解れば良いことになります。
買い物は楽天市場